Difference between revisions of "Literatura: ph"
(→Infekcyjność wirusa grypy w różnych pH (na podstawie )) |
|||
| Line 25: | Line 25: | ||
** Lee przy pH=7.9 | ** Lee przy pH=7.9 | ||
| − | * w T=4<sup>o</sup>C, w buforze fosforanowym | + | * w T=4<sup>o</sup>C, w buforze fosforanowym 0.1M stabilność wirusów PR8 i Lee była większa, gdy przechowywano je w stężeniu 2 mg/cm<sup>3</sup> niż w stężeniu 0.1 mg/cm<sup>3</sup>; w wyższym stężeniu wirusów, nawet po 2 miesiącach nie zauważono znaczącego spadku ich infekcyjności |
| − | W pH=5 infekcyjność wirusa gwałtownie spadała, co można | + | W pH=5 infekcyjność wirusa gwałtownie spadała, co można powiązać z denaturacją białek, czy kompleksów białek membranowych wirusa, w szczególności HA (co jednak istotne, funkcjonalność wirusa w organizmach, czyli fuzja błony wirusa z błoną komórki, zachodzi właśnie w kwaśnym środowisku, gdyż czynnikiem inicjującym fuzję jest rozplecenie trimeru HA). |
| − | < | + | |
| − | < | + | Warto też zwrócić uwagę na fakt, iż stabilność wirusa grypy, nawet w optymalnym pH (czyli ok 7) i temperaturze (T=4<sup>o</sup>C) także '''zależy od rodzaju i stężenia soli''' zawartych w środowisku<ref name="knight">C.A.Knight,"The stability of influenza virus in the presence of salts", (1944)</ref>. Knight<ref name="knight"/> badał stabilność wirusa PR8 w powyższych warunkach w [http://en.wikipedia.org/wiki/Buffer_solution buforach] boranowym (0.1 M), fosforanowym (ten ostatni w stężeniach 0.001, 0.01, 0.1 i 1 M) i [http://en.wikipedia.org/wiki/Barbital barbitalowym] (0.1 M), w wodzie destylowanej oraz w soli fizjologicznej (niebuforowanej). Wirus był najstabilniejszy w buforach: |
| + | |||
| + | * boranowym | ||
| + | * fosforanowym 0.1 M | ||
| + | * barbitalowym, | ||
| + | |||
| + | w których to zachował aktywność przez kilka tygodni. | ||
| + | |||
| + | W roztworze soli niebuforowanej wirus szybko tracił aktywność niezależnie od pH. Jak się okazało, aktywność częściowo zdezaktywowanego wirusa udało się zwiększyć 10-1000 krotnie poprzez dodawanie do roztworu 0.1 M buforu fosforanowego. | ||
===Stabilność trimeru HA w różnych pH i różnych temperaturach=== | ===Stabilność trimeru HA w różnych pH i różnych temperaturach=== | ||
Revision as of 13:36, 4 July 2008
| Moduł Socjo | Literatura wirusologiczna, czyli infekcyjność vs: | |
|---|---|
| Bieżące wyniki |
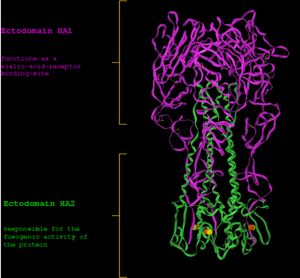
Stabilność/infekcyjność wirusa grypy w roztworach o różnych współczynnikach pH badano już w latach 30' XX w. Pierwsze badania, przeważnie na zwierzętch (np myszkach) dotyczyły infekcyjności konkretnych roztworów wirusa[1][2][3][4], współczesne badania dotyczą przed wszystkim zmian strukturalnych kompleksów białkowych w błonie wirusa, towarzyszących zmianie pH. Trimer hemaglutyninowy (HA) odgrywa bowiem istotną rolę w procesie fuzji błony wirusa z błoną komórki[5][6] [7][8][9][10].
Infekcyjność wirusa grypy w różnych pH (na podstawie [1])
Prace z przełomu 30' i 40' lat XX w. wskazują na stabilność wirusa grypy w pH 7-9[2], 7-7.5[3], 7[4]. Miller[1] przebadał 3 szczepy wirusów grypy: PR8 (wirus grypy A), Lee (wirus grypy B) i wirus świni w temperaturze 23 i 4oC w różnych stałych pH od 3 do 11. Z jego badań wynika iż:
- w T=23oC, wirus PR8 jest najbardziej stabilny w pH=6-7; po 10 dniach jego infekcyjność wynosi jeszcze 10% (badania prowadzone na myszkach, 10% może być jedną myszką z 10 badanych..).
- w T=4oC, wirus PR8 jest najbardziej stabilny w pH=6.5-7 ze wskazaniem na pH=7, przy czym w tej temperaturze jest bardziej stabilny niż w T=23.
Pozostałe (wybrane) wnioski autora:
- infekcyjność w buforach: tylko fosforanowym < Gly + NaCl < fosforanowy + Gly + NaCl; (jak się wydaje, glicyna chroni wirus)
- w buforze fosforanowym największą stabilność wirusy osiągały:
- PR8 przy pH=6.5-7
- świni przy pH=7-7.9
- Lee przy pH=7.9
- w T=4oC, w buforze fosforanowym 0.1M stabilność wirusów PR8 i Lee była większa, gdy przechowywano je w stężeniu 2 mg/cm3 niż w stężeniu 0.1 mg/cm3; w wyższym stężeniu wirusów, nawet po 2 miesiącach nie zauważono znaczącego spadku ich infekcyjności
W pH=5 infekcyjność wirusa gwałtownie spadała, co można powiązać z denaturacją białek, czy kompleksów białek membranowych wirusa, w szczególności HA (co jednak istotne, funkcjonalność wirusa w organizmach, czyli fuzja błony wirusa z błoną komórki, zachodzi właśnie w kwaśnym środowisku, gdyż czynnikiem inicjującym fuzję jest rozplecenie trimeru HA).
Warto też zwrócić uwagę na fakt, iż stabilność wirusa grypy, nawet w optymalnym pH (czyli ok 7) i temperaturze (T=4oC) także zależy od rodzaju i stężenia soli zawartych w środowisku[11]. Knight[11] badał stabilność wirusa PR8 w powyższych warunkach w buforach boranowym (0.1 M), fosforanowym (ten ostatni w stężeniach 0.001, 0.01, 0.1 i 1 M) i barbitalowym (0.1 M), w wodzie destylowanej oraz w soli fizjologicznej (niebuforowanej). Wirus był najstabilniejszy w buforach:
- boranowym
- fosforanowym 0.1 M
- barbitalowym,
w których to zachował aktywność przez kilka tygodni.
W roztworze soli niebuforowanej wirus szybko tracił aktywność niezależnie od pH. Jak się okazało, aktywność częściowo zdezaktywowanego wirusa udało się zwiększyć 10-1000 krotnie poprzez dodawanie do roztworu 0.1 M buforu fosforanowego.
Stabilność trimeru HA w różnych pH i różnych temperaturach
Bibliografia
- ↑ 1.0 1.1 1.2 Miller, 1944, "Influence of pH and of certain other conditions on the stability of the infectivity and red cell agglutinating activity of influenza virus"
- ↑ 2.0 2.1 Andrews, C. H., and Smith, W., Brit. J. Exp. Path., 18, 43, (1937)
- ↑ 3.0 3.1 Ostrovskaya, S. M., Czalkina, O. M., and Oleehnowiteh, S. B., Arch. sc. biol., 52, 31,(1938)
- ↑ 4.0 4.1 Stock, C. C., and Francis, T., Jr., J. Exp. Med.,71,661,(1940)
- ↑ Steinhauer et al, PNAS, 88, 11525-11529, (1991)
- ↑ Korte et al, J Biol Chem,272,9764,(1997)
- ↑ Epand, Epand, Biochem. J., 365, 841,(2002)
- ↑ Remeta et al, Biochemistry (2002), 41, 2044
- ↑ Huang et al, Bioph J, 82, p1050,(2002)
- ↑ Rachakonda et al, FASEB, 21, p996, (2007)
- ↑ 11.0 11.1 C.A.Knight,"The stability of influenza virus in the presence of salts", (1944)